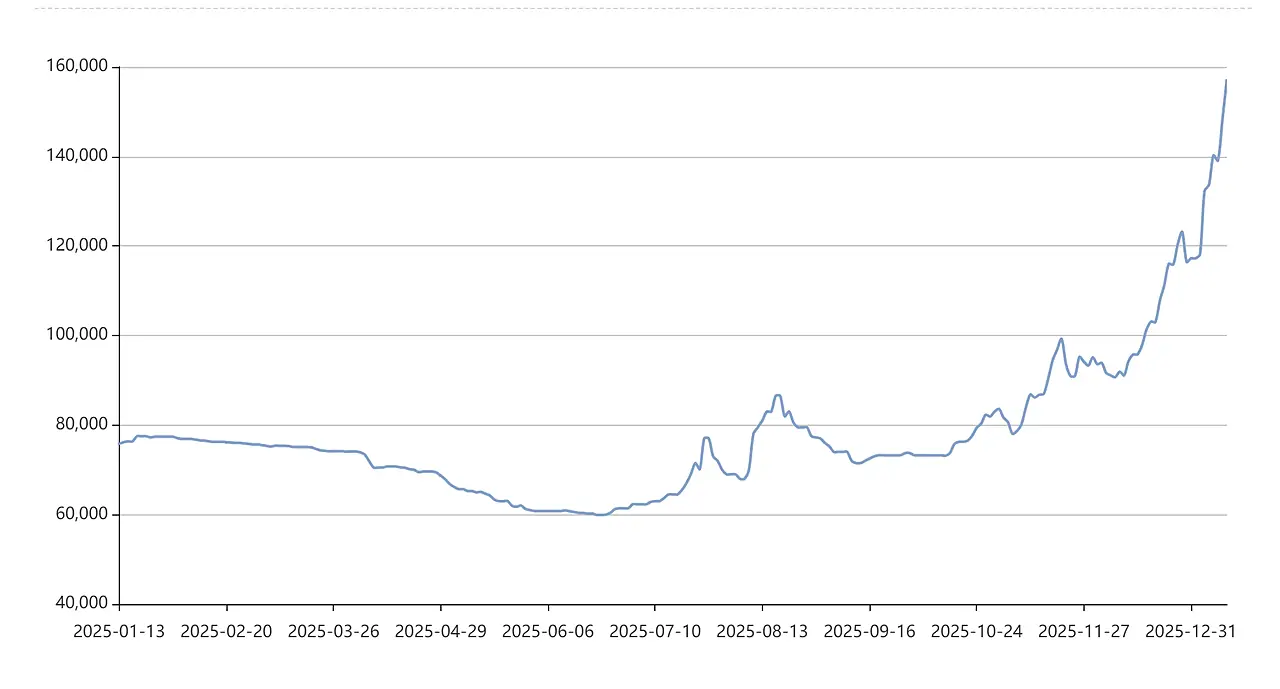
Como demanda del mercado de baterías de iones de litio continúa creciendo, han surgido problemas como la escasez de recursos de litio y el aumento de los precios.
Litio y sodio, Ambos metales alcalinos en el grupo IA de la tabla periódica, compartir propiedades físicas y químicas similares, Teóricamente haciéndolos adecuados como portadores de iones de metal en baterías secundarias. Batería de iones de sodio (Luz) compartir mecanismos similares de almacenamiento de energía que la batería de iones de litio, con capacidades y potencial específicos aceptables. Por lo tanto, Los SIB se consideran una alternativa viable a las baterías de iones de litio y se han convertido en un foco clave de investigación y desarrollo.
Estructura básica de la batería de iones de sodio
La estructura de la batería de iones de sodio es esencialmente la misma que la de la batería de iones de litio, que consiste principalmente en electrodo positivo, electrodo negativo, electrólito, separador, y coleccionista actual.
Basado en si los componentes de una batería de iones de sodio participan directamente en la reacción electroquímica, se pueden dividir en materiales activos e inactivos.. Los materiales activos incluyen el material de electrodo positivo, el material de electrodo negativo, y el material electrolítico. Los materiales inactivos incluyen el separador, el coleccionista actual, agente conductor, y carpeta.
La estructura y las propiedades del Materiales de electrodos positivos y negativos En una batería de iones de sodio, determine el rendimiento de almacenamiento de sodio de toda la batería. El electrólito actúa como un medio para el flujo de iones entre los electrodos positivos y negativos, permitiendo que los iones de sodio se muevan entre los electrodos mientras evitan el flujo directo de electrones. El separador separa los electrodos positivos y negativos, prevenir cortocircuitos mientras permite el transporte de iones. El coleccionista actual recoge y transmite electrones.
Principio de trabajo de batería de iones de sodio
La batería de iones de sodio no solo comparte una estructura similar a la batería de iones de litio, pero también operar esencialmente los mismos principios. Ambos funcionan por iones que se insertan y se eliminan de los electrodos positivos y negativos de la batería..
El principio de funcionamiento de la batería de iones de sodio es que los iones de sodio se mueven reversiblemente entre los electrodos positivos y negativos a través del electrolito, acompañado del flujo de electrones a través de un circuito externo. Este proceso se puede dividir en dos fases: Carga y descarga.
Cargando
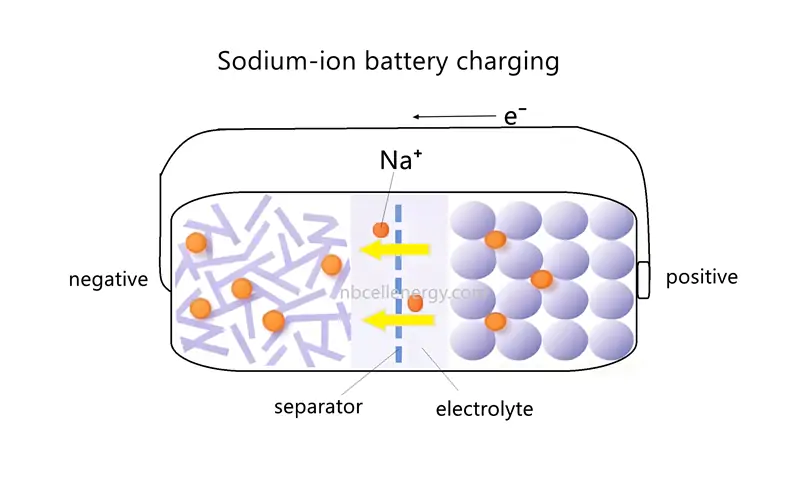
Cuando se carga la batería de iones de sodio, El electrodo positivo actúa como el ánodo (Donde ocurre una reacción de oxidación), y el electrodo negativo actúa como el cátodo (donde ocurre una reacción de reducción).
Durante este proceso, Una fuente de alimentación externa aplica un voltaje, Conducir iones de sodio (Na⁺) Desde el electrodo positivo a través del electrolito hasta el electrodo negativo. El flujo de electrones del electrodo positivo al electrodo negativo a través de un circuito externo. El material de electrodo negativo acepta iones de sodio del electrodo positivo y los electrones del circuito externo. Los iones de sodio están integrados en la estructura del electrodo negativo, y los electrones ingresan al electrodo negativo a través del circuito externo, Mantener saldo de carga.
Descarga
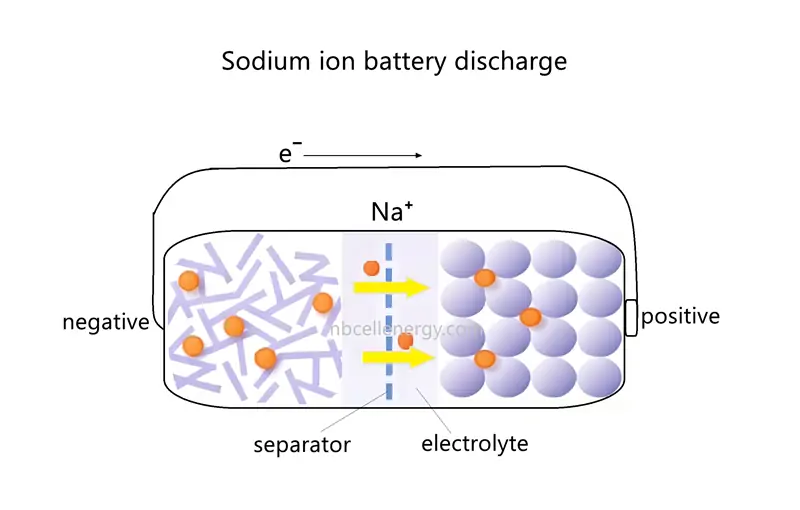
Durante el alta, El electrodo negativo de la batería de iones de sodio actúa como el ánodo (Donde ocurre una reacción de oxidación), y el electrodo positivo actúa como el cátodo (donde ocurre una reacción de reducción).
El proceso de descarga de la batería de iones de sodio es el reverso del proceso de carga. Los átomos de sodio almacenados en el material de electrodo negativo pierden electrones, formando iones de sodio (Na⁺). Estos iones de sodio se mueven del electrodo negativo al electrodo positivo a través del electrolito. El flujo de electrones del electrodo negativo al electrodo positivo a través de un circuito externo, Alimentación de dispositivos conectados. Los iones de sodio ingresan a la estructura cristalina del electrodo positivo a través del electrolito, mientras que los electrones ingresan al electrodo positivo a través del circuito externo, Mantener saldo de carga.
Proceso electroquímico
El movimiento de iones de sodio y electrones en baterías de iones de sodio se basa en varios procesos electroquímicos clave:
Intercalación/desintercalización: En la mayoría de las baterías de iones de sodio, Tanto el cátodo como los materiales del ánodo son en capas o porusas, Capaz de almacenar reversiblemente iones de sodio en sus redes de cristal. Por ejemplo, Los ánodos de carbono duro tienen una estructura desordenada que acomoda los iones de sodio, Mientras que los cátodos de óxido en capas (como nani₀.₅mn₀.₅o₂) Permita que los iones de sodio se muevan dentro y fuera del espacio entre capas.
Reacciones redox: Metales de transición (como Ni, Minnesota, y Fe) En el cátodo se someten a reacciones de oxidación y reducción para equilibrar la intercalación y liberación de iones de sodio. Por ejemplo, en nafepo₄, La pareja redox Fe²⁺/Fe³⁺ impulsa las reacciones electroquímicas.
Transporte iónico: El electrolito debe tener una alta conductividad iónica para permitir un transporte de iones de sodio eficiente. Los electrolitos comunes incluyen hexafluorofosfato de sodio (Bol) disuelto en solventes orgánicos como el carbonato de etileno (CE) y carbonato de propileno (ordenador personal). Electrolitos de estado sólido, como la alúmina β de sodio, también se están explorando para mejorar la seguridad.
Interfase de electrolito sólido (SER): Durante el primer ciclo de carga, Una película delgada de SEI se forma en la superficie del ánodo debido a la descomposición de electrolitos. Esta película pasiva el ánodo, prevenir una mayor degradación de electrolitos mientras permite el transporte de iones de sodio. Debido al mayor tamaño de iones na⁺, La película SEI en la interfase de electrolitos sólidos (Luz) es menos estable que en las baterías de iones de litio, planteando un desafío para la vida en bicicleta.