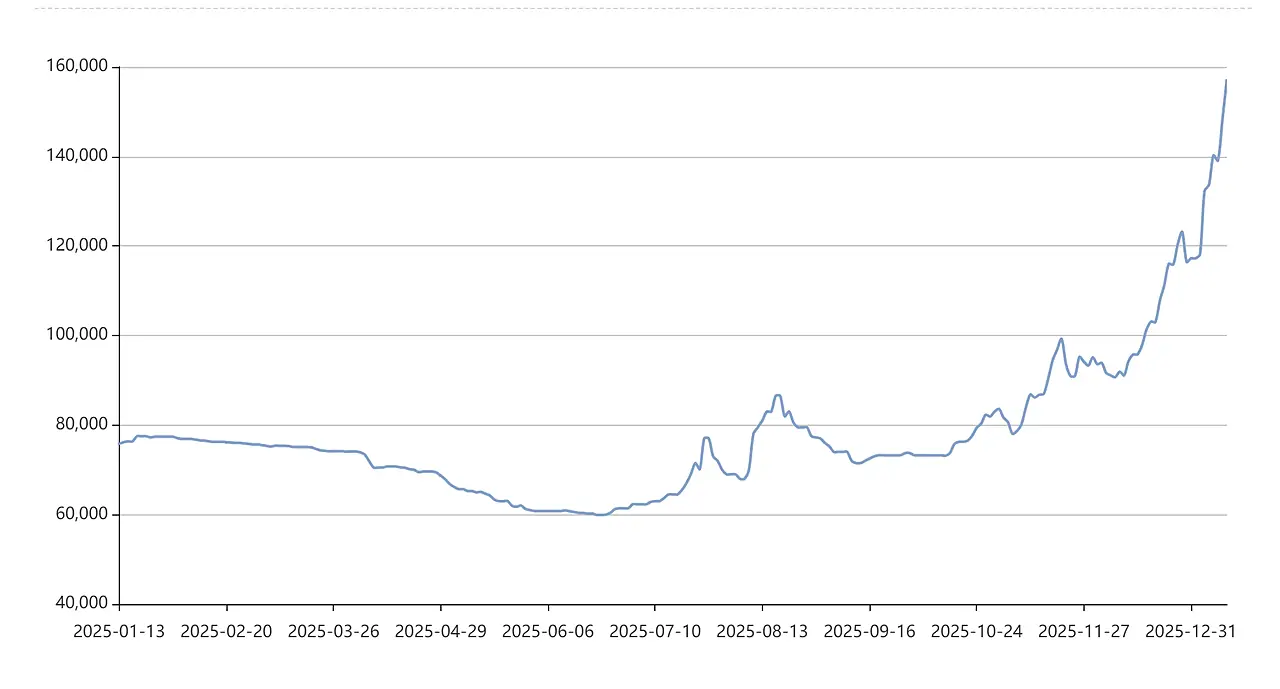
كطلب في السوق بطاريات الليثيوم أيون يستمر في النمو, ظهرت مشاكل مثل نقص موارد الليثيوم وارتفاع أسعارها تدريجياً.
الليثيوم والصوديوم, كل من المعادن القلوية في المجموعة IA من الجدول الدوري, مشاركة الخصائص الفيزيائية والكيميائية المماثلة, من الناحية النظرية ، جعلها مناسبة كحاملات أيون معدنية في البطاريات الثانوية. بطارية الصوديوم أيون (ضوء) مشاركة آليات تخزين الطاقة المماثلة كبطارية ليثيوم أيون, تفاخر بقدرات وإمكانات محددة مقبولة. لذلك, تعتبر SIBs بديلاً قابلاً للتطبيق لبطاريات الليثيوم أيون وأصبحت محورًا رئيسيًا للبحث والتطوير.
الهيكل الأساسي لبطارية أيون الصوديوم
بنية بطارية الصوديوم أيون هي نفسها في الأساس مثل بطارية الليثيوم أيون, يتكون في المقام الأول من القطب الإيجابي, القطب السلبي, المنحل بالكهرباء, فاصل, والمجمع الحالي.
بناءً على ما إذا كانت مكونات بطارية الصوديوم أيون تشارك مباشرة في التفاعل الكهروكيميائي, يمكن تقسيمها إلى مواد نشطة وغير نشطة. تشمل المواد النشطة مادة القطب الإيجابي, مادة القطب السلبي, ومواد المنحل بالكهرباء. تشمل المواد غير النشطة الفاصل, جامع الحالي, وكيل موصل, والوثق.
هيكل وخصائص مواد الإلكترود الإيجابية والسلبية في بطارية الصوديوم أيون ، حدد أداء تخزين الصوديوم للبطارية بأكملها. ال المنحل بالكهرباء يعمل كوسيلة لتدفق الأيونات بين الأقطاب الإيجابية والسلبية, السماح لأيونات الصوديوم بالتحرك بين الأقطاب الكهربائية مع منع التدفق المباشر للإلكترونات. ال فاصل يفصل الأقطاب الإيجابية والسلبية, منع دوائر قصيرة مع السماح للنقل الأيوني. ال جامع الحالي يجمع وينقل الإلكترونات.
مبدأ عمل بطارية أيون الصوديوم
لا تشترك بطارية الصوديوم أيون في بنية مماثلة لبطارية الليثيوم أيون, ولكن تعمل أيضًا على نفس المبادئ. كلاهما يعملان بواسطة أيونات إدراج وإزالة من الأقطاب الكهربائية الإيجابية والسلبية للبطارية.
مبدأ عمل بطارية الصوديوم أيون هو أن أيونات الصوديوم تتحرك بشكل عكسي بين الأقطاب الإيجابية والسلبية من خلال المنحل بالكهرباء, يرافقه تدفق الإلكترونات من خلال دائرة خارجية. يمكن تقسيم هذه العملية إلى مرحلتين: الشحن والتفريغ.
الشحن
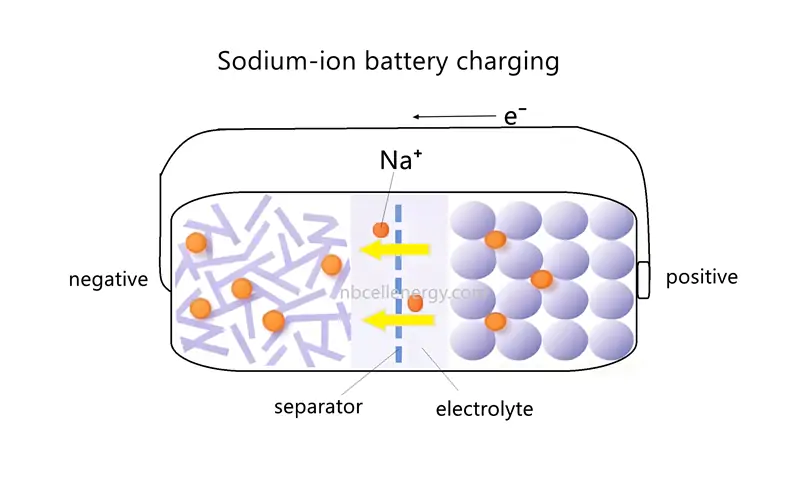
عندما يتم شحن بطارية الصوديوم أيون, يعمل القطب الإيجابي كأنود (حيث يحدث تفاعل الأكسدة), ويعمل القطب السلبي ككاثود (حيث يحدث تفاعل التخفيض).
خلال هذه العملية, يطبق مصدر طاقة خارجي الجهد, قيادة أيونات الصوديوم (نا) من القطب الإيجابي عبر المنحل بالكهرباء إلى القطب السلبي. تتدفق الإلكترونات من القطب الإيجابي إلى القطب السلبي عبر دائرة خارجية. تقبل مادة القطب السلبي أيونات الصوديوم من القطب الإيجابي والإلكترونات من الدائرة الخارجية. أيونات الصوديوم مضمنة في بنية القطب السلبي, وتدخل الإلكترونات القطب السلبي من خلال الدائرة الخارجية, الحفاظ على توازن الشحن.
التفريغ
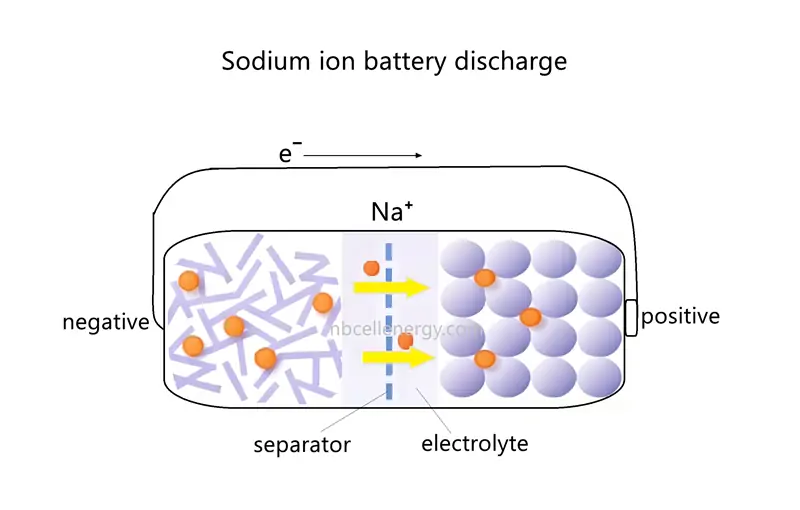
أثناء التفريغ, يعمل القطب السلبي لبطارية الصوديوم أيون كأنود (حيث يحدث تفاعل الأكسدة), ويعمل القطب الإيجابي ككاثود (حيث يحدث تفاعل التخفيض).
عملية تصريف بطارية الصوديوم أيون هي عكس عملية الشحن. ذرات الصوديوم المخزنة في مادة القطب السلبي تفقد الإلكترونات, تشكيل أيونات الصوديوم (نا). تنتقل أيونات الصوديوم هذه من القطب السلبي إلى القطب الإيجابي من خلال المنحل بالكهرباء. تتدفق الإلكترونات من القطب السلبي إلى القطب الإيجابي من خلال دائرة خارجية, تشغيل الأجهزة المتصلة. تدخل أيونات الصوديوم بنية الكريستال للقطب الإيجابي من خلال المنحل بالكهرباء, بينما تدخل الإلكترونات القطب الإيجابي من خلال الدائرة الخارجية, الحفاظ على توازن الشحن.
العملية الكهروكيميائية
تعتمد حركة أيونات الصوديوم والإلكترونات في بطاريات الصوديوم أيون على العديد من العمليات الكهروكيميائية الرئيسية:
intercalation/defintercalation: في معظم بطاريات الصوديوم أيون, كل من مواد الكاثود والأنود هي طبقات أو مسامية, قادرة على تخزين أيونات الصوديوم بشكل عكسي في شبكاتها البلورية. على سبيل المثال, أنودات الكربون الصلبة لها بنية مضطربة تستوعب أيونات الصوديوم, بينما كاثود أكسيد الطبقات (مثل nani₀.₅mn₀.₅o₂) السماح لأيونات الصوديوم بالانتقال إلى الداخل والخروج من مساحة الطبقة البينية.
تفاعلات الأكسدة: المعادن الانتقالية (مثل ني, MN, و Fe) في الكاثود يخضع لتفاعلات الأكسدة والخفض لموازنة intercalation وإطلاق أيونات الصوديوم. على سبيل المثال, في Nafepo₄, يدفع زوجان الأكسدة والاختزال.
النقل الأيوني: يجب أن يكون للكهرباء الموصلية أيونية عالية لتمكين النقل الأيوني الصوديوم الفعال. تشمل الشوارد الشائعة سداسي فوسفات الصوديوم (صَحن) يذوب في المذيبات العضوية مثل كربونات الإيثيلين (EC) والبروبيلين كربونات (الكمبيوتر الشخصي). الشوارد الصلبة الحالة, مثل الصوديوم β-alumina, يتم استكشافها أيضًا لتحسين السلامة.
الطور المنحل بالكهرباء الصلبة (يكون): خلال دورة الشحن الأولى, يتشكل فيلم SEI رقيق على سطح الأنود بسبب تحلل المنحل بالكهرباء. هذا الفيلم يمرر الأنود, منع المزيد من تدهور المنحل بالكهرباء مع السماح بنقل أيون الصوديوم. بسبب حجم أيونات na⁺ الأكبر, فيلم SEI في الطور الإلكتروليت الصلب (ضوء) أقل استقرارًا من بطاريات الليثيوم أيون, تشكل تحديا لدوران الحياة.